Nuove prospettive nella gestione della sepsi, in particolare dell’AKI settica e il ruolo specifico della membrana dialitica in tale contesto sono stati presentati recentemente da Giuseppe Castellano al 61° congresso nazionale SIN (Società Italiana di Nefrologia). I risultati presentati mostrano la capacità della nuova membrana in PMMA per terapie continue nell’inibire l’attivazione del sistema del complemento nel quadro clinico di AKI settica indotta da LPS, con conseguente riduzione della transizione del danno renale acuto (AKI) a danno renale cronico (CKD), aprendo di fatto un nuovo orizzonte nel trattamento e nella gestione dell’AKI settica.
Download PdfAKI settica: dalla fisiopatologia alla membrana dialitica come strategia di intervento
Fisiopatologia dell’AKI settica
La sepsi è definita come una disfunzione d’organo potenzialmente letale causata da una risposta disregolata dell’ospite ad un’infezione (1) mentre lo shock settico è un particolare quadro clinico di sepsi in cui le anomalie circolatorie e cellulari/metaboliche derivanti sono così critiche da comportare un incremento significativo di mortalità (1). La risposta immunitaria nell’ospite viene
indotta quando i recettori dell’immunità innata (PRR) sulla superficie delle cellule immunitarie riconoscono i patterns molecolari associati ai patogeni (PAMP), come il lipopolisaccaride (LPS) e i patterns molecolari associati al danno (DAMP), che vengono rilasciati in risposta allo stimolo infiammatorio. Può ingenerarsi una risposta disregolata dell’ospite che può condurre ad una disfunzione d’organo potenzialmente letale ed ad una sindrome da disfunzione multiorgano (MODS). L’endotossina (definita
anche LPS) è il più potente trigger della cascata settica ed è stata pertanto studiata e definita in decenni di ricerca come
un target terapeutico.
Toraymyxin® è un Dispositivo Medico costituito da una cartuccia in cui è immobilizzata la polimixina B, rendendo disponibili le potenti capacità di neutralizzazione dell’endotossina da parte della polimixina B attraverso un trattamento di emoperfusione. Numerosi studi clinici hanno dimostrato che il trattamento di polimixina B in emoperfusione (PMX-HP) migliora la funzionalità d’organo e l’outcome dei pazienti settici. La terapia di PMX-HP può contribuire anche a un effetto di prevenzione di danno renale acuto (AKI) indotto da sepsi, in quanto riduce l’attività dei fattori circolanti pro-apoptotici renali (2).
Nel contesto di AKI ed AKI settica, una crescente evidenza clinica indica che l’attivazione del sistema del complemento contribuisce alla sua patogenesi (3). Gli effetti a breve termine dell’attivazione del sistema complemento (intradialitica) includono la stimolazione dello stato pro-infiammatorio e dei processi di coagulazione (4).
Terapia sostitutiva renale continua con PMMA e risposta immunitaria
Il Prof. Castellano ha presentato i risultati di una ricerca condotta in un recente studio collaborativo volto ad identificare nuovi meccanismi patogenetici in un modello suino di AKI indotto da LPS. In particolare, l’obiettivo dei ricercatori è stato quello di
studiare la potenziale efficacia dell’emofiltrazione continua (CVVH) con membrana PMMA nel modulare l’attivazione immunitaria sistemica e tissutale in un modello suino di AKI indotta da LPS. I risultati presentati dimostrano che un trattamento sostitutivo renale continuo (CRRT) con membrana in Polimetilmetacrilato (PMMA), contrariamente alla membrana convenzionale in Polysulfone (PS), conduce al recupero della funzionalità renale, migliorando lo stato di oligo-anuria e ipotensione con riduzione del fabbisogno di
catecolamine negli animali con AKI settica. Rispetto al gruppo di trattamento con membrana in PS, PMMA-CRRT ha ridotto anche l’infiltrazione di cellule infiammatorie nel parenchima renale, ridotto la fibrosi renale acuta ed la formazione trombi glomerulari.
I ricercatori hanno ulteriormente analizzato questo effetto identificando che PMMA-CRRT riduce i depositi di PTX3 sulle cellule renali e l’attivazione locale del sistema del complemento. PMMA-CRRT inoltre riduce l’attivazione sistemica del sistema del complemento abrogando l’attivazione sia della via classica sia di quella alternativa. Il PMMA-CRRT contribuisce a diminuire i livelli sierici di LBP e di sCD40. Il profilo dell’ espressione genica del genoma delle PBMCs nel modello animale suino, ha dimostrato che LPS attiva i leucociti circolanti; nel gruppo di animali tratatti con PMMA-CRRT si è riscontrata invece un’evidente riduzione di tale attivazione.
Implicazioni per i pazienti COVID-19
I risultati presentati hanno inevitabilmente anche implicazioni per i pazienti affetti da COVID-19 e insorgenza di AKI. È ormai noto che COVID-19 nella fase acuta è associata ad una risposta disregolata dell’ospite ad un’infezione, proprio come accade nella sepsi. Inoltre, i pazienti ricoverati in ospedale per periodi prolungati possono essere suscettibili ad infezioni sovrapposte, aumentando il rischio di insorgenza e progressione di sepsi e shock settico con insufficienza multiorgano (5). Fino al 25% dei pazienti critici con diagnosi di COVID-19 può sviluppare AKI (6). Ed è stato evidenziato come in questi pazienti vi sia attivazione importante del
sistema del complemento e come questo debba essere considerato un appropriato target di intervento terapeutico (7).
In un recente articolo pubblicato su Nature Reviews, la terapia di PMX-HP è raccomandata nei pazienti COVID-19 con shock settico, con infezioni batteriche da Gram-negativo sospette o confermate e alto livello di endotossinemia (8). Lo stesso gruppo di ricercatori ha recentemente pubblicato una flowchart di utilizzo di PMX-HP nei pazienti in shock settico (9) suggerendola come primo intervento complementare nelle condizioni cliniche descritte.
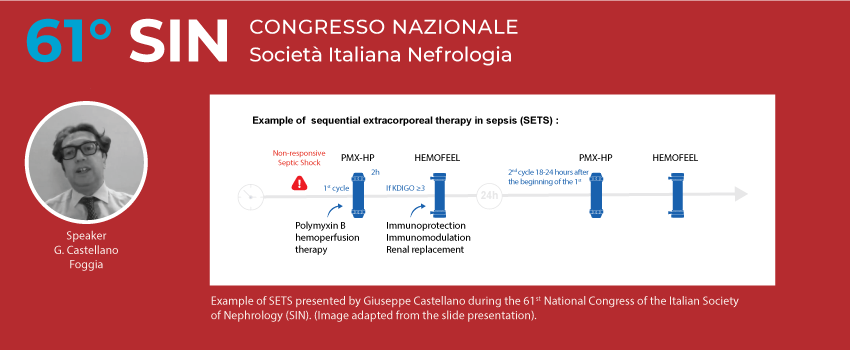
Un modello di intervento
Dai risultati presentati è chiaro che l’endotossina (LPS) induce una risposta immunitaria che può essere disregolata, non solo a livello sistemico, ma anche a livello specifico renale. È stato dimostrato che PMMA-CRRT attenua la transizione da AKI a CKD in un quadro clinico di AKI settica. Al fine di massimizzare la strategia di intervento terapeutico, è stato poi sviluppato e introdotto il concetto di terapia extracorporea sequenziale nella sepsi (SETS). Più precisamente, nei pazienti con shock settico che sviluppano AKI con necessità di supporto renale, la terapia sequenziale che considera PMMA-CRRT a seguito di PMX-HP, sembra essere un approccio razionale e pragmatico. Inoltre, la nuova tecnologia offerta da una macchina per CRRT specificamente progettata, garantisce la gestione automatizzata della terapia sequenziale (SETS) con la combinazione delle 2 proposte terapeutiche:
- PMX-HP: primo trattamento per ottenere la massima neutralizzazione di endotossina e l’aferesi di cellule immunitarie attivate (monociti e neutrofili attivati)
- PMMA-CRRT: secondo trattamento da eseguire in caso di AKI con necessità di RRT, consentendo la massima emocompatibilità evitando l’attivazione del sistema del complemento e promuovendo l’adsorbimento di mediatori pro-infiammatori comprese le citochine.
Il webinar può essere visto on-demand dai partecipanti registrati sul website del congresso.
Clicca qui per vedere il contenuto.
Riferimenti
- Singer M, Deutschman CS, Seymour C, et al. The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA : the journal of the American Medical Association. 2016;315(8):801-10.
- Cantaluppi V, Assenzio B, Pasero D, Romanazzi GM, Pacitti A, Lanfranco G, et al. Polymyxin-B hemoperfusion inactivates circulating proapoptotic factors. Intensive care medicine. 2008;34(9):1638-45.
- Franzin R, Stasi A, Fiorentino M, Stallone G, Cantaluppi V, Gesualdo L, et al. Inflammaging and Complement System: A Link Between Acute Kidney Injury and Chronic Graft Damage. Frontiers in immunology. 2020;11:734.
- Poppelaars F, Faria B, Gaya da Costa M, Franssen CFM, van Son WJ, Berger SP, et al. The Complement System in Dialysis: A Forgotten Story? Frontiers in immunology. 2018;9:71.
- Noris M, Benigni A, Remuzzi G. The case of complement activation in COVID-19 multiorgan impact. Kidney international. 2020;98(2):314-22.
- Fanelli V, Fiorentino M, Cantaluppi V, Gesualdo L, Stallone G, Ronco C, et al. Acute kidney injury in SARS-CoV-2 infected patients. Critical care (London, England). 2020;24(1):155.
- Risitano AM, Mastellos DC, Huber-Lang M, Yancopoulou D, Garlanda C, Ciceri F, et al. Complement as a target in COVID-19? Nat Rev Immunol. 2020;20(6):343-4.
- Ronco C, Reis T. Kidney involvement in COVID-19 and rationale for extracorporeal therapies. Nature reviews Nephrology. 2020.
- De Rosa S, Villa G, Ronco C. The golden hour of polymyxin B hemoperfusion in endotoxic shock: The basis for sequential extracorporeal therapy in sepsis. Artificial organs. 2019.